免疫治疗靶点后起之秀:TIGIT

免疫检查点抑制剂已经成为癌症治疗的热门领域,其中以PD-1/PD-L1抑制剂为代表,已引起国内外药企的竞相布局。但PD-1/PD-L1抑制剂在临床应用中仅有少数患者得到良好治疗,而且还出现耐药性及严重不良反应,因此急需找到新的靶点来弥补PD-1/PD-L1的不足,TIGIT、LAG-3、TIM-3等新兴免疫检查点渐渐崭露头角。
TIGIT(T cell immunoreceptor with Ig and ITIM domain, T细胞免疫球蛋白和ITIM结构域)是T细胞和自然杀伤细胞(NK细胞)共有的抑制性受体,可抑制NK细胞和T细胞对肿瘤细胞的杀伤作用,是近年来较为火热的新兴免疫检查点。从目前较好的临床研究结果看,TIGIT有望与PD-1/PD-L1抑制剂形成组合拳以阻断TIGIT信号通路,有可能增强机体对癌细胞的免疫反应,提高抗肿瘤活性。迈杰转化医学针对TIGIT抑制剂的药物临床研究已经积累了丰富的生物标志物解决方案经验。
01 TIGIT简介及信号通路
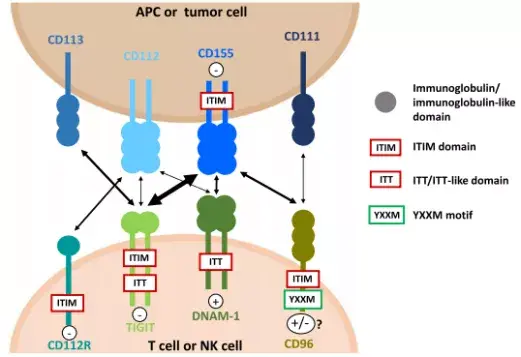
TIGIT是脊髓灰质炎病毒受体(PVR)家族的一种抑制性受体,也称为WUCAM,Vstm3,VSIG,是Ig超家族的一种受体,在限制适应性和固有免疫方面起着关键作用[1-3]。TIGIT在自然杀伤(NK)细胞和T细胞上表达(包括活化的CD4+ T,CD8+ T,Tregs,Type 1 regulatory T, Foliicular helper T),而其配体包括:CD155(即PVR),CD112(即PVRL2)和CD113,在抗原呈递细胞(APC)或肿瘤细胞上表达。在TIGIT/DNAM-1通路中,TIGIT和CD112R、DNAM-1共享配体CD112,和DNAM-1竞争结合
CD155[4-5]。TIGIT、CD112R和CD155通过细胞质尾将抑制信号传递至细胞,DNAM-1则传递激活信号。人CD96和小鼠CD96均包含ITIM结构域,但人CD96同时也包含YXXM基序。研究已显示CD96抑制小鼠T细胞和NK细胞,而YXXM基序可能会导致CD96在人和小鼠细胞中传递的信号差异(图1)。
02 TIGIT的作用机制
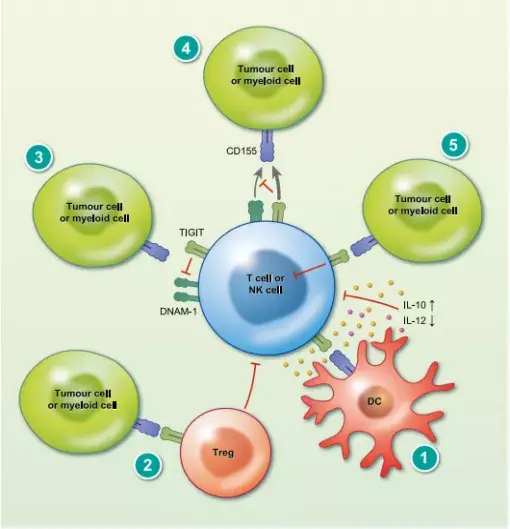
据报道,TIGIT通过多种机制抑制T细胞和NK细胞。
(1)在TIGIT-CD155相互作用后,表达CD155的树突状细胞(DC)可能变得耐受,DC细胞的耐受性体现在:抗原递呈下降,共刺激分子的低表达以及与抗炎细胞因子(如 IL-10)分泌有关的促炎细胞因子(如白细胞介素IL-12)的减产。总之,这些树突状细胞 (DC) 功能的改变导致T细胞活化受损。
(2)TIGIT在调节性T细胞(Treg)中经常上调,使Treg呈现高度抑制性。
(3)TIGIT会破坏细胞表面的DNAM-1顺式同源二聚化,从而阻止DNAM-1与CD155 的相互作用。
(4)与DNAM-1相比,TIGIT以更高的亲和力结合CD155,与CD155的相互作用可能胜过DNAM-1。
(5)TIGIT还可以通过其胞质尾将抑制信号直接传递给T细胞和NK细胞。此外,在Treg上表达时,TIGIT可增强Treg抑制功能,从而可能抑制多种免疫细胞[6-8](图2)。
03 TIGIT抑制剂的临床经验
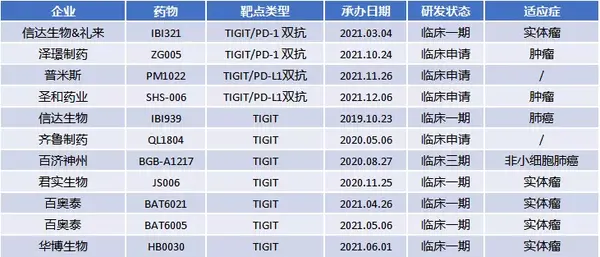
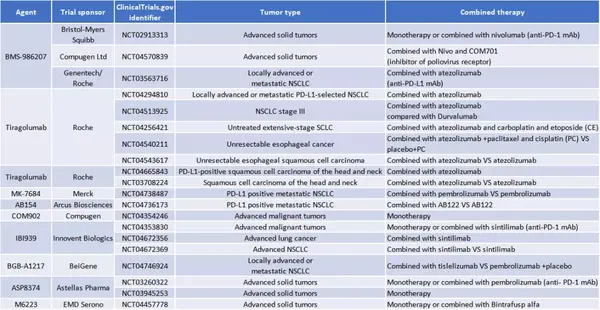
TIGIT靶点已成为将来免疫检查位点抑制剂的新贵,虽然目前全球尚无TIGIT抗体获批上市,但是已经陆续有十余款TIGIT抗体进入临床。国际制药巨头Roche,BMS,MSD等对此靶点均有布局,尤其以Roche的投入力度最大(表1-2)。
04 新药进展:Tiragolumab&Ociperlimab
2021年12月,罗氏和百济神州分别公布了靶向TIGIT联合疗法的研究成果和NMPA临床试验获批的消息。这些消息令人鼓舞,联用PD-(L)1+TIGIT的组合疗法,有可能成为解决癌症治疗短板的新方法。
距离Tiragolumab获“突破性疗法”认定仅一年不到,2021年12月10日,罗氏公布了靶向TIGIT的新型癌症免疫疗法“Tiragolumab联合PD-L1药物Tecentriq”作为一线疗法,治疗PD-L1阳性转移性非小细胞肺癌(NSCLC)患者的2期临床研究CITYSCAPE的最新数据(表3a-b)。
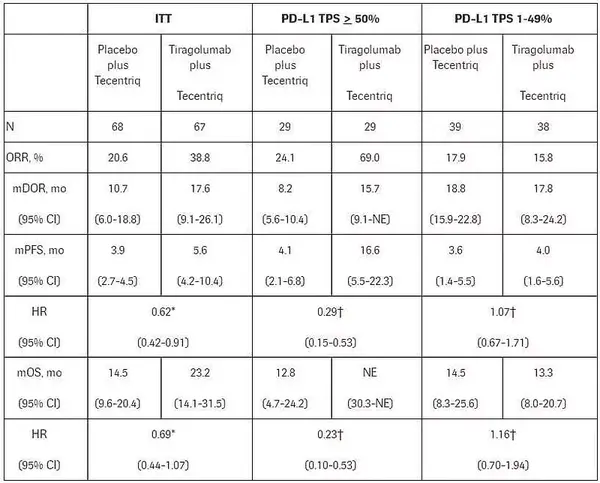
更新的数据主要是在中位随访时间为2.5年时,相比于Tecentriq单药治疗,Tiragolumab联合Tecentriq组合疗法使患者获得无进展生存期(PFS)的显著与持续改善:
(1)在意向治疗(ITT)人群中,与Tecentriq单药治疗(中位PFS=3.9个月)相比,Tiragolumab联合Tecentriq组合疗法使患者疾病进展或死亡的风险降低了38%(中位PFS=5.6个月),并提高了总缓解率(ORR)(38.8% VS 20.6%)。
(2)在PD-L1高表达患者中,与Tecentriq单药治疗(中位PFS=4.1个月)相比,组合疗法使患者疾病进展或死亡风险的风险降低了71%(中位PFS=16.6个月),ORR显著改善(69% VS 24.1%)。
(3)在总生存期(OS)的试验次要终点上,Tiragolumab联合Tecentriq组合疗法也为ITT人群带来获益,中位OS为23.2个月,而对照组为14.5个月。
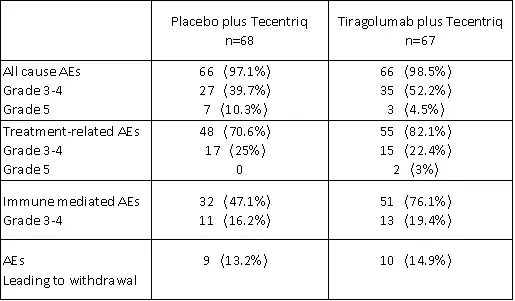
此外,在安全性方面,与单独使用Tecentriq相比,两种免疫疗法联合使用时,3级或以上不良事件(AE)的发生率相近(22.4% VS 25%)。Tiragolumab与Tecentriq的组合耐受性良好,与单独的Tecentriq治疗相比,并没有安全性风险的增加。
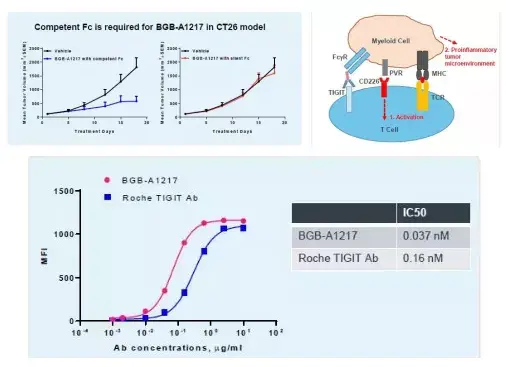
12月17日,百济神州PD-1+TIGIT联合治疗弥漫性大B细胞淋巴瘤(DLBCL)的临床试验获得NMPA默示许可。12月20日,百济神州与诺华达成合作协议:诺华将获得百济神州TIGIT抗体的美国、加拿大、欧洲多国及日本的权益,并将支付3亿美元预付款,6或7亿美元的额外付款,18.95亿美元里程碑金额以及20-25%的销售分成。这是百济神州继替雷利珠单抗之后,与诺华达成的又一笔交易,也是双方合作的进一步深化。本次合作的重点Ociperlimab(BGB-A1217)是一款在研的强效TIGIT抑制剂,由百济神州自主研发并将在全球范围内进行开发。作为一款在研人源化 IgG 1 单克隆抗体,Ociperlimab具有完善的Fc段功能,对于TIGIT抗体的抗肿瘤活动能力至关重要。而此次获批的DLBCL临床实验,为百济神州PD-1+TIGIT首次进军血液瘤的研究领域。TIGIT抗体BGB-A1217,保留对抗肿瘤活性必要的Fc效应,在临床前实验中表现出比罗氏Tiragolumab强4倍的抗肿瘤活性(图3)。
05 MEDx生物标志物解决方案
深入研究TIGIT介导的免疫反应调节,将有助于针对癌症患者设计TIGIT阻断剂的优化组合策略,进一步开发靶向TIGIT疗法来造福更多的癌症患者。表4中列出了目前TIGIT研究中的生物标志物的研究报道。
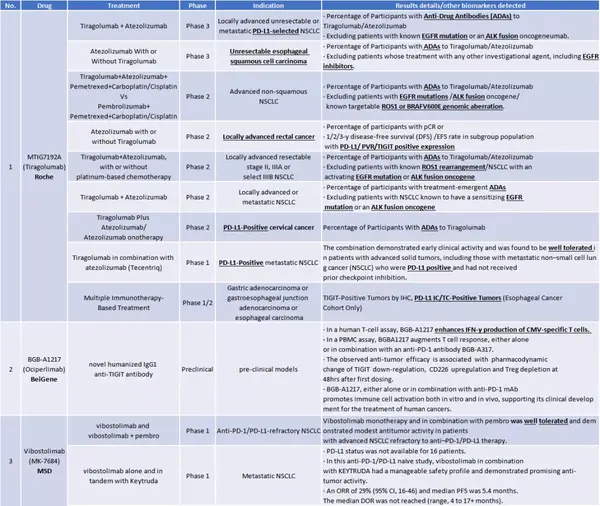
图4a-d展示了Arcus biosciences的TIGIT抗体AB154的研究,包含了采用IHC检测CD155在NSCLC等多种癌症中的表达,流式方法检测外周血各种免疫细胞亚型中TIGIT和PD1的表达,流式方法检测抗体占位等。
A. IHC测定检测CD155表达
结果显示了 NSCLC 和其他肿瘤中癌细胞、血管和三级淋巴结构 (TLS) 的膜和细胞质定位(箭头表示阳性染色)。
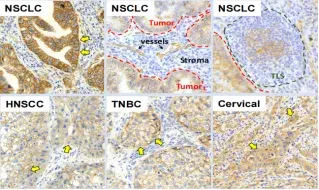
B. 流式检测TIGIT和PD-1
肿瘤内有抗原经历的CD8+T细胞高度表达TIGIT和PD-1。
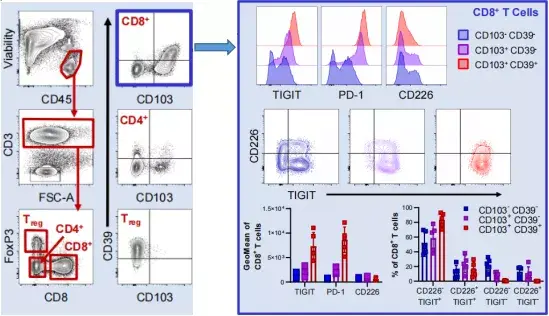
C. 流式细胞术检测外周血中TIGIT的表达
患者和健康供体在外周血淋巴细胞中具有相似的TIGIT表达,包括CD8+和 CD8-T细胞、NK细胞和NKT细胞。

D. 流式检测受体覆盖率
在所有入选受试者的每个波谷时间点初始给药后,在所有表达 TIGIT 的外周淋巴细胞中均观察到完全受体覆盖。
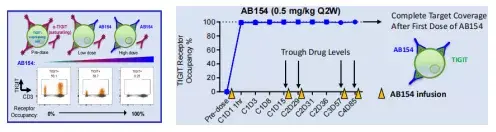
以上研究推动了TIGIT抑制剂相关的生物标志物检测和伴随诊断试剂的开发。针对患者分层及各类指标的研究,迈杰转化医学可以提供TIGIT抑制剂治疗中生物标志物研究的整体解决方案(表5)。
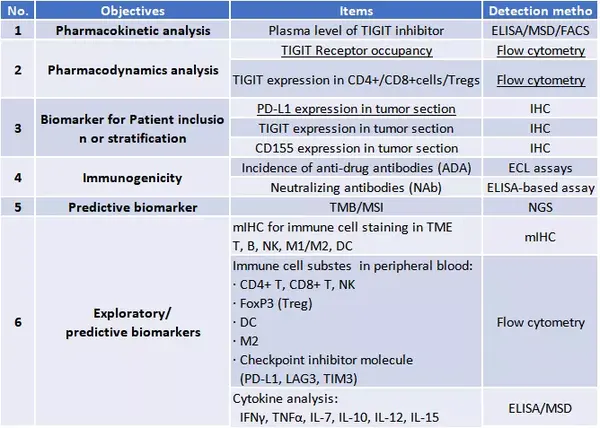
References
[1] Yu X, Harden K, Gonzalez LC et al. The surface protein TIGIT suppresses T cell activation by promoting the generation of mature immunoregulatory dendritic cells. Nat Immunol 2009; 10:48–57.
[2] Boles KS, Vermi W, Facchetti F et al. A novel molecular interaction for the adhesion of follicular CD4 T cells to follicular DC. Eur J Immunol 2009; 39:695–703.
[3] Levin SD, Taft DW, Brandt CS et al. Vstm3 is a member of the CD28 family and an important modulator of T-cell function. Eur J Immunol 2011; 41:902–15.
[4] Zhu Y, Paniccia A, Schulick AC et al. Identification of CD112R as a novel checkpoint for human T cells. J Exp Med 2016; 213:167–76.
[5] Levy O, Chan C, Cojocaru G et al. Abstract 581: Discovery and development of COM701, a therapeutic antibody targeting the novel immune checkpoint PVRIG. Cancer Res 2017; 77(13 Supplement):581.
[6] Harjunpää* H , Guillerey C. TIGIT as an emerging immune checkpoint[J]. Clinical and Experimental Immunology, 200: 108–119.
[7] Joller N, Lozano E, Burkett PR et al. Treg cells expressing the coinhibitory molecule TIGIT selectively inhibit proinflammatory Th1 and Th17 cell responses. Immunity 2014; 40:569–81.
[8] Fuhrman CA, Yeh WI, Seay HR et al. Divergent phenotypes of human regulatory T cells expressing the receptors TIGIT and CD226. J Immunol (Balt) 2015; 195:145–55.
[9] Ge Z, Peppelenbosch M P, Sprengers D, et al. TIGIT, the next step towards successfulcombination immune checkpoint therapy in cancer[J]. Frontiers in Immunology,2021, 12.
[10] Anderson A E , Direnzo D , Lee S , et al. Abstract 1557: Characterization of AB154, a humanized anti-TIGIT antibody, for use in combination studies[C] Proceedings: AACR Annual Meeting 2019; March 29-April 3, 2019; Atlanta, GA. 2019.
往期回顾
1、众多创新药企布局免疫检查点LAG-3,下一个PD-L1?
2、PD-L1检测服务与伴随诊断产品全面布局,迈杰转化医学多维度赋能合作伙伴3、肌动蛋白结合蛋白1(FSCN1):潜力生物标志物及药物开发靶点?
4、DNA 复制调节因子 MCM6:一种新兴的癌症生物标志物和药物靶点5、Claudin 18.2:创新药企必争之靶点,迈杰转化医学鼎力支持药企临床试验入组及伴随诊断开发
央视《匠心》栏目视角看迈杰转化医学